
“得福组合”:贝莫苏拜单抗是一种新型的人源化lgG1亚型PD-L1单抗,安罗替尼是一种小分子多靶点酪氨酸激酶受体抑制剂,安罗替尼通过调控肿瘤微环境重编程联合免疫检查点抑制剂实现协同增效的抗肿瘤作用。
一、临床指南推荐-食管癌篇
1、CSCO食管癌诊疗指南(2025版)[1]
推荐意见:对于存在化疗禁忌或拒绝化疗的患者,也可考虑安罗替尼联合贝莫苏拜单抗治疗。
2、中国食管癌放射治疗指南(2025版)[2]
中国食管癌放射治疗指南(2024版)[3]
推荐意见:
安罗替尼+贝莫苏拜单抗(鳞癌,一线,Ⅲ级推荐,3类证据)
安罗替尼+贝莫苏拜单抗+紫杉醇+顺铂(鳞癌,一线,Ⅱ级推荐)
3、食管癌免疫检查点抑制剂临床应用全程管理专家共识(2024版)[4]
共识意见:安罗替尼联合贝莫苏拜单抗用于晚期ESCC的一线治疗有较好的疗效及可控的毒性,但仍需进一步验证。
核心研究数据解读
贝莫苏拜单抗联合安罗替尼一线治疗晚期食管鳞癌:一项单臂、多中心、开放标签的Ⅱ期临床研究[5]
数据来源:2025年《Molecular Cancer》
Highlights:ALTER-E003研究评估贝莫苏拜单抗联合安罗替尼去化疗方案一线治疗晚期食管鳞癌的有效性和安全性,经确认的ORR达到56.5%,中位PFS为15.74个月,中位OS为20.57个月,≥3级TRAEs发生率为28.3%。该方案延长受试者生存获益的同时,降低了不良事件发生率,为晚期食管鳞癌一线治疗提供了新的思路。
研究设计
本研究是一项单臂、多中心、开放标签的Ⅱ期临床研究
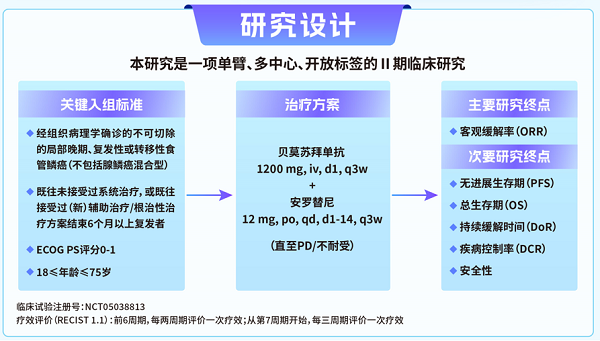
疗效数据
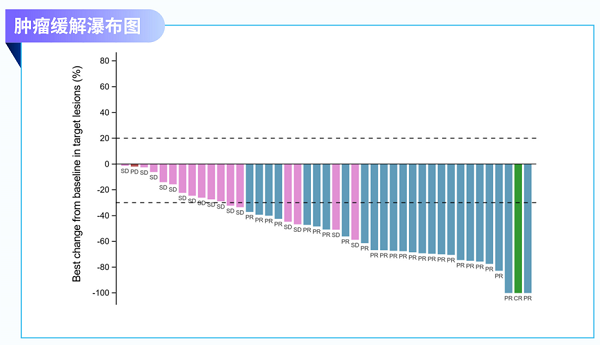
经确认的ORR为56.5%(95%CI: 41.1%-71.1%)
DCR为91.3%(95%CI: 79.2%-97.6%)
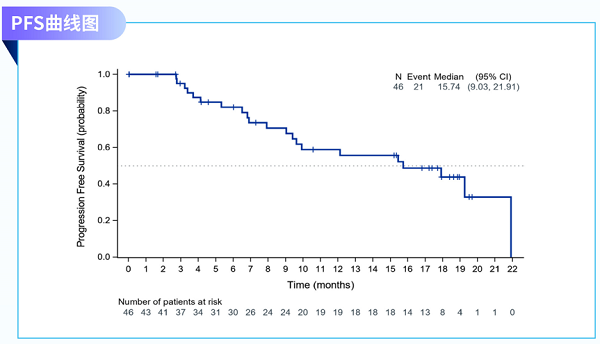
中位PFS为15.74个月(95%CI: 9.03-21.91)
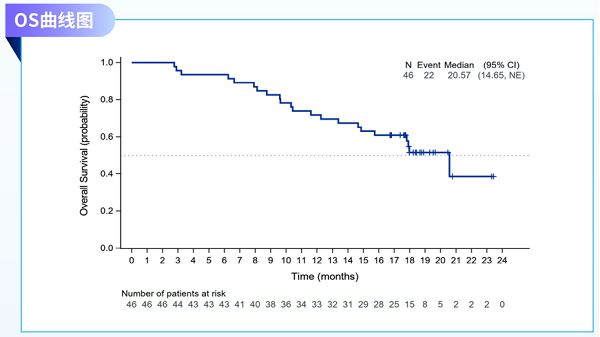
中位OS为20.57个月(95%CI: 14.65-不可评估[NE])
安全性数据
安全性方面:整体TRAEs的发生率为93.5%,≥3级TRAEs的发生率为28.3%,常见的≥3级TRAEs包括高血压(10.9%)、低钠血症(4.3%)、中性粒细胞计数降低(4.3%),蛋白尿、掌跖红肿综合征和上消化道出血各1例(2.2%),未发生治疗相关的死亡事件。
二、临床指南推荐-胆道系统肿瘤篇
1、CSCO胆道恶性肿瘤诊疗指南(2025版)[6]
CSCO胆道恶性肿瘤诊疗指南(2024版)[7]

核心研究数据解读
贝莫苏拜单抗联合安罗替尼二线治疗晚期胆道系统肿瘤的Ib期研究及生物标志物分析[8]
来源:2022年《Hepatology》, Epub ahead of print
Highlights:本项数据评估贝莫苏拜单抗联合安罗替尼二线治疗晚期胆道系统肿瘤的疗效及安全性,ORR为21.21%,DCR为72.73%,中位PFS为6.24个月,中位OS为15.77个月,受试者耐受性良好。为胆道系统肿瘤的二线治疗提供了有潜在应用价值的新策略,同时发现了有望用于指导临床治疗的潜在分子标志物。
研究设计
本研究是同期分别在两个中心开展的两项Ib期临床研究的汇总分析
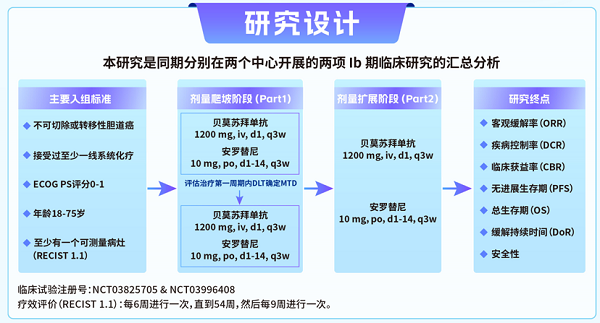
疗效数据
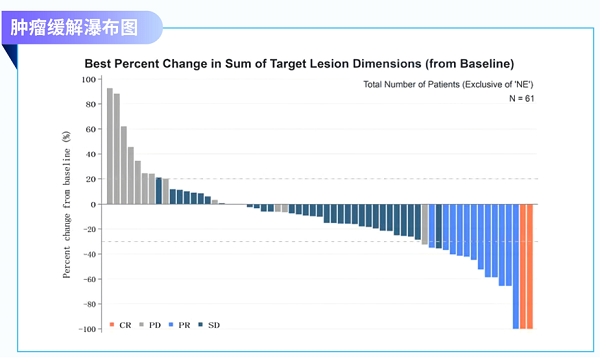
ORR为21.21%(95%CI,12.11%-33.02%)
DCR为72.73%(95%CI,60.36%-82.97%)
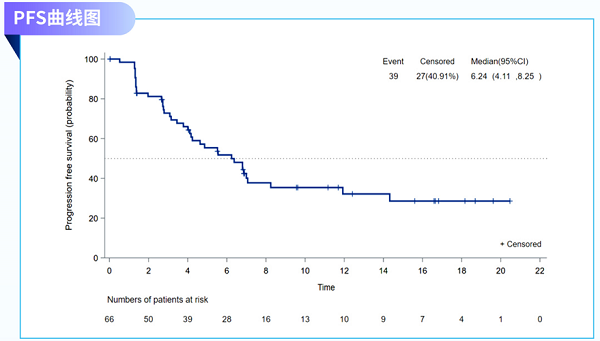
中位PFS为6.24个月(95%CI, 4.11-8.25)
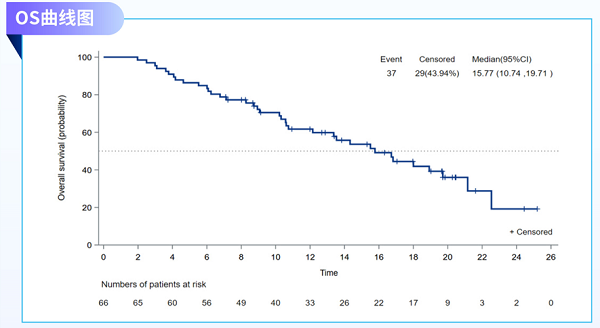
中位OS为15.77个月(95%CI, 10.74-19.71)
安全性数据
安全性方面:最常见的治疗相关不良事件(TRAEs)是甲状腺功能减退(54.55%)、白细胞减少(42.42%)、天冬氨酸氨基转移酶升高(40.91%)、腹泻(40.91%)和胆红素升高(39.39%)。≥3级TRAEs的发生率为25.76%,常见为天冬氨酸氨基转移酶升高(7.58%)、丙氨酸氨基转移酶升高(6.06%)和高血压(6.06%)。
参考文献:
[1] 中国临床肿瘤学会指南工作委员会. CSCO食管癌诊疗指南2025[M]. 北京: 人民卫生出版社, 2025.
[2] 中国食管癌放射治疗指南[J].国际肿瘤学杂志,2026,53(01):1-15.
[3] 中国食管癌放射治疗指南[J].国际肿瘤学杂志,2025,53(01):3-22.
[4] 食管癌免疫检查点抑制剂临床应用全程管理专家共识[J].中国医学前沿杂志(电子版),2024,16(7):1-21.
[5] Meng,X., et al. Anlotinib combined with benmelstobart as a chemo-free first-line treatment in advanced esophageal squamous cell carcinoma: an exploratory multicenter, single-arm phase II clinical trial,Molecular Cancer,2025,24(1):175.
[6] 中国临床肿瘤学会指南工作委员会. 胆道恶性肿瘤诊疗指南2025[M]. 北京: 人民卫生出版社, 2025.
[7] 中国临床肿瘤学会指南工作委员会. 胆道恶性肿瘤诊疗指南2024[M]. 北京: 人民卫生出版社, 2024.
[8] Zhou, J., et al. Phase Ib study of anlotinib combined with TQB2450 in pretreated advanced biliary tract cancer and biomarker analysis,Hepatology, 2023, 77 (1): 65-76.
*本资料为专业医学资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考,非广告用途;任何处方请参考产品最新详细处方资料

